 Las clorofilas a y b son pigmentos de color verde, formadas por cuatro anillos pirrolicos con diversos substituyentes laterales. Los pirroles, con sus átomos de nitrógeno unen un cation Mg 2+ en el centro, formado por un anillo complejo de estructura casi plana. Las clorofilas a y b se diferencian por sus substituyentes del anillo pirrolico III: la clorofila a tiene un grupo metilo como radical y la clorofila b tiene un grupo aldehído.
Las clorofilas a y b son pigmentos de color verde, formadas por cuatro anillos pirrolicos con diversos substituyentes laterales. Los pirroles, con sus átomos de nitrógeno unen un cation Mg 2+ en el centro, formado por un anillo complejo de estructura casi plana. Las clorofilas a y b se diferencian por sus substituyentes del anillo pirrolico III: la clorofila a tiene un grupo metilo como radical y la clorofila b tiene un grupo aldehído.Los carotenoides son de color rojo, naranja o amarillo. Químicamente son poliisoprenoides de 40 átomos de carbono y según si contienen o no átomos de oxígeno en su estructura se llaman carotenos ( sin oxígeno ) o xantofilas ( con oxígeno ).
Una de las técnicas mas usadas para la separación de componentes es la cromatografia (proceso de separacion de mezclas complejas mediante particiones entre una fase fluida y movil y una fase estacionaria )
Práctica de laboratorio en relación a este tema:
Primeramente se extraen cuatro tipos de pigmentos vegetales:
- Clorofilas a y b
- Xantofilas
- Carotenos
Todos ellos tienen carácter apolar, aunque su grado de polaridad varia en función de su composición química. Así pues, hay un gradiente de polaridad desde el mas al menos apolar.
Los objetivos son claros; determinar cuantitativamente los pigmentos presentes en los tejidos vegetales, separar los componentes mayoritarios de los pigmentos fotosinteticos mediante cromatografia de papel y comparar los contenidos en pigmentos de diferentes especies, edad o estado de las hojas.
Determinación cuantitativa de los pigmentos fotosinteticos ( Clorofilas y carotenoides )
Procedimiento:
Se ha de procurar trabajar en condiciones de poca luz y frio, los matraces y el mortero se pondrán en hielo. Con un " Traucador " se hacen dos o tres cortes de la hoja. Ha de procurarse evitar los nervios de la hoja. Se determina el peso fresco de la hoja y la area utilizada en los cortes.
Se colocan los fragmentos en un mortero y se añade un poco de acetona 80%. A continuación se tritura la hoja en el mortero. Se considera que hemos separado todos los pigmentos cuando los restos de las hojas son completamente transparentes.
Se filtra el contenido del mortero con la ayuda de un papel de filtro dentro de un embudo y se hace pasar al matraz aforado. Se enrasa con el diluyente usado, acetona 80% en nuestro caso.
La medida de las absorbancias (cantidad de intensidad de luz que absorbe la muestra); se hace con el espectrofotometro. Se lee a las longitudes de onda: 663.6, 646,6 y 470,0 nm.
Resultados:
Para determinar la cantidad de clorofil·la a y b presentes a la hoja se utilizan las
equaciones de Porra y para loss contenidos de carotenoides, la equacion de Lichtenthaler y
Wellburn :
Clorofil·la a (µg/ml) = 12,25·(A663,6) – 2,55·(A646,6)
Clorofil·la b (µg/ml) = 20,31·(A646,6) – 4,91·(A663,6)
Clorofil·la total a+b (µg/ml) = 17,76·(A646,6) + 7,34·(A663,6)
Carotenoides (µg/ml) = (1000·A470 – 3,27·[chl a] – 104·[chl b])/227
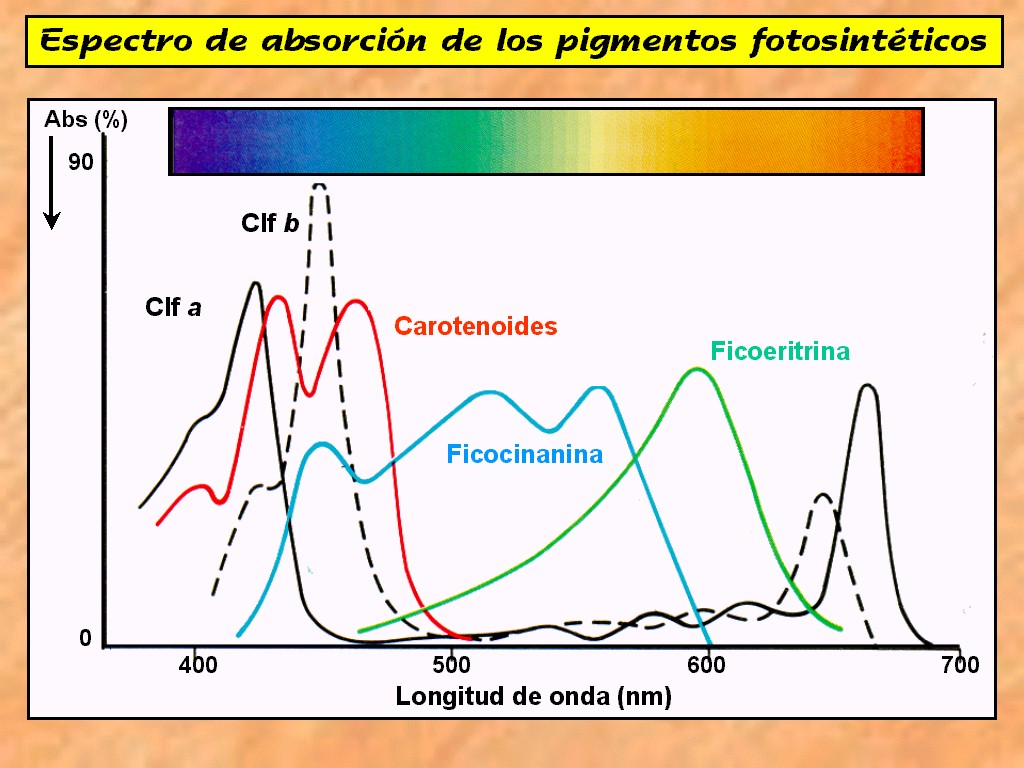
Espectros de absorción característicos de ciertos pigmentos:
Podemos apreciar a través de este gráfico que las clorofilas absorben en el verde por tanto emiten esa luz ( es la luz reflejada la de color verde ). Igual que la Ficoeritrina. La ficocinanina absorbe en el azul y los carotenoides en el rojo.
No hay comentarios:
Publicar un comentario